HIPEC при онкологических заболеваниях
Гипертермическая внутрибрюшинная (интраперитонеальная) химиотерапия (hyperthermic intraperitoneal chemotherapy, сокращенно HIPEC) представляет собой современный метод лечения при онкологических заболеваниях, сопровождающихся поражением брюшины – оболочки, выстилающей стенки брюшной полости и покрывающей находящиеся в ней органы. У таких пациентов сильно ухудшается прогноз, а классическая системная химиотерапия (когда препарат вводят внутривенно) помогает слабо и вызывает тяжелые побочные эффекты при повышении доз.
HIPEC состоит из двух этапов. Сначала проводят хирургическое вмешательство и удаляют все видимые опухолевые очаги, а затем брюшную полость промывают раствором химиопрепарата, нагретым до 42 °C. За счет того, что химиопрепарат находится только в брюшной полости и почти не проникает в кровоток, можно существенно увеличить дозу, не боясь серьезных побочных эффектов. А высокая температура помогает лекарственному средству лучше проникать в опухолевые очаги и уничтожать злокачественные клетки.
История появления метода HIPEC
Хотя гипертермическая внутрибрюшинная химиотерапия сама по себе является новой методикой, ее предыстория началась почти сто лет назад. В 1937 году американский акушер-гинеколог Джо Винсент Мейгс впервые описал циторедуктивную операцию при раке яичников. Он предложил в случаях, когда опухоль нельзя убрать полностью, удалять хотя бы как можно больший ее объем. Это должно было улучшать состояние пациенток и продлевать их жизнь.
В 60–70-х годах хирурги окончательно убедились в целесообразности такого подхода и стали широко применять агрессивные циторедуктивные операции при раке яичников. В это время американский врач Кент Гриффит обратил внимание, что выживаемость пациенток сильно зависит от того, какой объем опухолей оставлен после операции – оптимально не более 1,6 см в диаметре. Одновременно было обнаружено, что если ввести после циторедукции в брюшную полость химиопрепарат и повысить температуру, то результат получается еще лучше. Первые эксперименты проводили на собаках, а затем эту методику стали применять и у онкологических больных.
Изначально новый метод лечения назвали термотрансфузионной инфильтрацией (TIFS). Врачи обнаружили, что в брюшную полость можно безопасно вводить дозы химиопрепаратов, в 30 раз превышающие таковые при внутривенной терапии.
Свой окончательный вид методика HIPEC обрела в 2016 году, когда Lotti M. et al. предложили использовать во время гипертермической химиотерапии лапароскопический подход. После циторедуктивной операции брюшную полость зашивают, оставляя отверстия для трубок, через которые подают нагретый раствор химиопрепарата. За счет этого меньше теряется тепло и химиопрепарат удобнее равномерно распределить по брюшной полости.
В чем отличия метода HIPEC от химиотерапии и его преимущества?
Главные отличия HYPEC при лечении заболеваний в онкологии от классической химиотерапии в том, что химиопрепарат вводят только в брюшную полость, а не системно в кровоток, используют более высокие дозы и нагревают раствор лекарства. Отсюда следуют преимущества методики:
- Химиопрепарат в более высокой дозе эффективнее уничтожает раковые клетки.
- Около 90% препарата остается в брюшной полости и не поступает в кровоток, поэтому сильно снижается риск побочных эффектов.
- Нагревание само по себе поражает раковые клетки и улучшает проникновение препарата в опухолевые очаги за счет расширения кровеносных сосудов. Злокачественные новообразования как бы получают удар сразу с двух сторон.
- Лечение включает одну операцию вместо длительного курса химиотерапии.
- Главное – это, конечно же, эффективность. В научных работах многократно доказано, что HIPEC существенно повышает выживаемость пациентов.
Когда может быть полезна интраперитонеальная гипертермическая химиотерапия?
Гипертермическую интраперитонеальную химиотерапию применяют у онкологических пациентов с канцероматозом (раковым поражением) брюшины – смертельно опасным состоянием с плохим прогнозом. Другие методы лечения помогают таким больным лишь в небольшой степени и ненадолго. HIPEC – единственный эффективный метод.
Что представляет собой брюшина, и чем опасно ее поражение опухолевыми клетками?
Брюшина представляет собой серозную оболочку. Внешне она выглядит как тонкая пленка. В ней выделяют две части:
- Париетальная – покрывает изнутри стенки брюшной полости.
- Висцеральная – служит оболочкой для внутренних органов.
Брюшина выполняет важные функции: она обеспечивает поддержку для внутренних органов, их свободное скольжение относительно друг друга во время дыхания, в процессе пищеварения, в ней проходят нервы, кровеносные и лимфатические сосуды.
Метастазирование рака – сложный процесс. Многие злокачественные клетки отделяются от первичной опухоли и мигрируют в организме. Но многие из них в итоге погибают. Некоторые находят благоприятные условия в различных органах и дают начало метастатическим очагам. Такой «благодатной почвой» нередко становится брюшина. Некоторые злокачественные опухоли развиваются изначально в ней.
При канцероматозе функции брюшины нарушаются, в животе больного скапливается жидкость (асцит), его состояние значительно ухудшается, а прогноз становится неблагоприятным. Долгое время у врачей не было эффективного способа борьбы с этой проблемой. Теперь такой способ существует – это HIPEC.
Канцероматоз брюшины встречается при различных злокачественных опухолях:
- Первичные опухоли брюшины встречаются редко – их диагностируют у 7 человек из миллиона. Наиболее распространена серозная карцинома брюшины – она составляет 10% от всех злокачественных новообразований органов малого таза. Злокачественная мезотелиома встречается реже, но часто приводит к гибели пациентов. Намного чаще перитонеальный канцероматоз вызван метастазами рака из других органов.
- При раке яичников метастазы в брюшине обнаруживают в 75% случаев на момент установления диагноза. Более чем в половине случаев они возникают одновременно с первичной опухолью.
- При раке толстой и прямой кишки – в 5–10% случаев на момент установления диагноза.
- При раке желудка – в 20–50% (в 14% случаев при первичном обращении к врачу).
- В 9% случаев канцероматоз брюшины вызывают метастазы из органов, находящихся за пределами брюшной полости. Среди них:
- рак молочной железы – 40,8%;
- рак легкого – 25,6%;
- меланома – 9,3%.
Показания
Чтобы HIPEC прошла без осложнений и помогла продлить жизнь пациента с канцероматозом, должны быть соблюдены три основных условия:
- Возможность удалить все крупные опухолевые очаги хирургически, а оставшиеся уничтожить нагретыми химиопрепаратами.
- Достаточно хорошее состояние пациента, чтобы он смог перенести такое серьезное хирургическое вмешательство.
- Отсутствие метастазов за пределами брюшной полости.
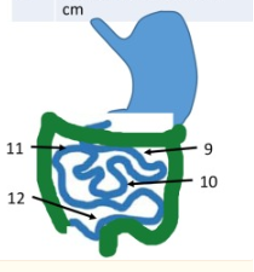
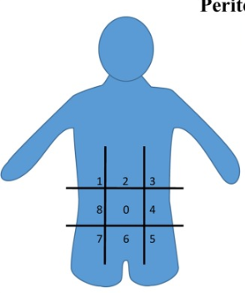
Всё это проверяют во время обследования. Чтобы оценить, насколько сильно рак успел распространиться в пределах брюшной полости, используют специальный индекс перитонеального канцероматоза. Брюшную полость делят на 13 областей и проверяют, сколько в каждой из них опухолевых очагов, какого они размера:
- центральная (синонимы: околопупочная, мезогастрий);
- правая подреберная;
- эпигастрий;
- левая подреберная;
- левая боковая;
- левая подвздошная;
- надлобковая (гипогастрий);
- правая подвздошная;
- правая боковая;
- верхняя часть тощей кишки;
- нижняя часть тощей кишки;
- верхняя часть подвздошной кишки;
- нижняя часть подвздошной кишки.
В зависимости от размеров самой крупной опухоли, каждая область получает определенное число баллов:
|
0 |
Опухолевые очаги отсутствуют |
|
1 |
Диаметр самой крупной опухоли до 0,5 см |
|
2 |
Диаметр самой крупной опухоли до 5 см |
|
3 |
Присутствует хотя бы один очаг более 5 см |
В целом же HIPEC чаще всего применяют для лечения канцероматоза брюшины, вызванного следующими злокачественными опухолями:
- рак надпочечников;
- рак аппендикса – червеобразного отростка слепой кишки;
- колоректальный рак (злокачественные новообразования толстой и прямой кишки);
- рак желудка;
- рак печени;
- злокачественная мезотелиома;
- рак яичников;
- рак поджелудочной железы;
- первичные опухоли брюшины.
Риски и противопоказания
В некоторых случаях гипертермическая внутрибрюшинная химиотерапия не помогает повысить показатели выживаемости, и в этих ситуациях она противопоказана:
- Неполная циторедукция – если во время хирургического вмешательства не удалось полностью удалить опухолевые очаги.
- Слишком обширное опухолевое поражение брюшины – об этом говорит индекс перитонеального канцероматоза более 20.
- Опухоль вторгается в корень брыжейки (складка брюшины, на которой подвешена кишка и в которой проходят кровеносные сосуды, нервы), печеночную ножку (пучок кровеносных сосудов, нервов и желчных протоков, выходящих из печени), забрюшинное пространство, мочевой пузырь.
Суть лечения в том, что во время операции хирург удаляет максимально возможное количество опухолевой ткани, а нагретый химиопрепарат уничтожает оставшиеся опухолевые клетки. Если этого заведомо не получится сделать, то и HIPEC не будет иметь смысла, не повлияет на прогноз, а лишь создаст для пациента риски.
Первый этап лечения – операция по удалению опухолевых очагов – серьезное хирургическое вмешательство, представляющее собой сильный стресс для организма и сопряженное с определенными рисками. Оно противопоказано людям с тяжелыми заболеваниями сердечно-сосудистой системы, легких, печеночной, почечной недостаточностью. Относительным противопоказанием является аллергическая реакция на противоопухолевые средства.
С наиболее высокими рисками связана циторедуктивная операция. Она сопровождается осложнениями, по некоторым данным, в 33% случаев. Хирургическое вмешательство может привести к таким состояниям, как:
- инфекционные осложнения;
- кровотечение;
- тромбозы;
- тромбоэмболия легочной артерии – состояние, при котором кусочек тромба отрывается, попадает в сосуды легких и вызывает симптомы, опасные для жизни;
- свищи – патологические сообщения между органами;
- панкреатит – воспаление поджелудочной железы.
На фоне сложных хирургических манипуляций, являющихся стрессом для организма, несколько повышается токсичность химиопрепаратов. Так, в 5,6% случаев наблюдаются побочные эффекты со стороны системы кроветворения (снижение уровней клеток крови), в 1,7% случаев – со стороны почек.
Восстановление после вмешательства происходит достаточно долго.
Как и любое лечение, HIPEC имеет риски и противопоказания. Однако плюсов у этой методики все же значительно больше, чем ограничений. Это единственная надежда для онкологических больных с канцероматозом брюшины. HIPEC помогает продлить их жизнь – в ряде случаев на долгие годы. Если у вас или вашего близкого диагностировали онкологическое заболевание с канцероматозом брюшины – запишитесь на прием к врачу-онкологу в клинике MAMMA. Наши специалисты обладают высоким уровнем экспертности в области применения HIPEC, они назначат обследование и расскажут, показан ли этот вид лечения в вашем случае.
Чтобы минимизировать риски, врач перед операцией должен тщательно оценить общее состояние здоровья пациента, учесть его возраст, стадию опухолевого процесса и степень распространения в брюшной полости, предполагаемый объем хирургического вмешательства.
Как проводится процедура?
Перед гипертермической внутрибрюшинной химиотерапией нужно провести тщательное предоперационное обследование в соответствии со стандартами Всемирной Организации Здравоохранения (ВОЗ). Врач должен подробно рассказать пациенту о предстоящем лечении, как оно будет проводиться, с какой целью, какой эффект ожидается, каковы риски. Пациент должен рассказать обо всех своих сопутствующих заболеваниях, лекарственных препаратах, которые он принимает, аллергических реакциях. Врач может отменить на время некоторые препараты – например, антикоагулянты («кроверазжижающие»), так как они повышают риск сильного кровотечения.
Лечение проводится в операционной под общим наркозом и продолжается в среднем 8–10 часов. Оно состоит из двух основных этапов: циторедуктивной операции и непосредственно HIPEC.
Этап I: циторедуктивная операция
Хирурги делают разрез и проводят ревизию – внимательно осматривают брюшную полость, все опухолевые очаги. Именно на этом этапе оценивают индекс перитонеального канцероматоза. Если он достаточно низкий, то переходят к циторедукции, а если выше критических значений – завершают операцию ввиду нецелесообразности иссечения опухолей и HIPEC.
Во время циторедуктивного вмешательства необходимо удалить все достаточно крупные – диаметром от 1–2 мм – опухолевые очаги. Это обязательное условие для того, чтобы всё последующее лечение было эффективным. Для этого нужно:
- Выполнить резекцию – удалить все части органов, пораженные злокачественным процессом.
- При обширном опухолевом поражении органа – удалить его полностью.
- Удалить пораженные лимфатические узлы.
- Удалить все пораженные участки брюшины.
Затем хирурги еще раз проводят ревизию, чтобы убедиться, что все опухоли удалены. Выполняют реконструкцию: сшивают концы кишечника или накладывают стомы (отверстия, соединяющие кишку с поверхностью кожи). После этого переходят к следующему этапу. Большой разрез больше не нужен – его зашивают.
Этап II: гипертермическая интраперитонеальная химиотерапия
После операции в стенке брюшной полости оставляют небольшие отверстия и вводят через них катетеры. Вторые концы этих катетеров подсоединены к специальному аппарату, через них в брюшную полость подают нагретый раствор химиопрепарата, так, чтобы он распределился равномерно. Это нужно, чтобы уничтожить опухолевые клетки, оставшиеся в организме больного. В противном случае они образуют новые очаги, и в лечении не будет смысла.
Гипертермическую внутрибрюшинную терапию проводят в течение 60–90 минут. Во время процедуры специальные датчики контролируют температуру, объем раствора, скорость его потока, давление. Когда промывание брюшной полости завершено, раствор препарата удаляют, вытаскивают катетеры и накладывают швы.
Результаты лечения и эффективность методики
При поражении брюшины метастазами рака продолжительность жизни пациентов в среднем составляет 6 месяцев, а при III и IV стадиях заболевания – всего 2–4 месяца. При первичных злокачественных опухолях брюшины медианная выживаемость ненамного выше – 11–17 месяцев. В то же время, по данным одного исследования 2005 года, медиана выживаемости при поражении раковыми клетками брюшины у пациентов с раком кишечника после применения HIPEC составила 21,8 месяца, то есть почти два года. Спустя 5 лет 19% пациентов остались в живых. А когда в 2008 году ученые проанализировали применение HIPEC у 1290 пациентов с разными злокачественными опухолями, пятилетняя выживаемость составила 37%.
Какие химиопрепараты используют во время HIPEC?
Для гипертермической внутрибрюшинной химиотерапии используют те же препараты, что и для системной терапии: митомицин С, цисплатин, доксорубицин, паклитаксел и иринотекан. Только применяются более высокие дозировки.
Что происходит после HIPEC?
После того как пациент перенес такое серьезное хирургическое вмешательство, его помещают в палату интенсивной терапии – в среднем на 2 суток. В это время медицинский персонал контролирует жизненные функции пациента, уровни электролитов и других веществ в крови. В общем госпитализация обычно длится 14–20 дней.
В послеоперационном периоде могут быть назначены некоторые лекарственные препараты:
- Внутривенные инфузии для восполнения жидкости и электролитов.
- Антибиотики для профилактики инфекционных осложнений.
- Обезболивающие для снятия болей. Иногда проводят эпидуральную анестезию – введение обезболивающих препаратов в позвоночный канал.
- При повышенном уровне глюкозы в крови вводят инсулин.
Питание зачастую поначалу внутривенное. Впоследствии пациент может принимать пищу самостоятельно. Этого нужно добиваться как можно быстрее, с учетом физиологических возможностей: чем раньше пищеварительная система начнет работать сама, тем быстрее восстановится ее нормальная функция.
При выписке из стационара врач дает пациенту рекомендации, назначает даты контрольных осмотров и обследований. Может быть назначен (и чаще всего его назначают) курс адъювантной химиотерапии, таргетной терапии, иммунотерапии.
В течение нескольких месяцев после операции могут возникать некоторые симптомы, но они считаются не осложнениями, а побочными эффектами. Это реакция организма на перенесенный во время операции стресс. Возможные проблемы: вздутие живота, запоры, диарея, депрессия, чувство усталости, нарушения сна, боли, тошнота, потеря веса. Если беспокоит что-то из перечисленного, нужно обратиться к врачу. Он назначит лечение, которое поможет нормализовать состояние.
Цены
В стоимость лечения входит цена операции и процедуры химиотерапии HIPEC, предварительная консультация врача и обследование, пребывание в стационаре, сопутствующие процедуры (например, введения тех или иных лекарственных препаратов). Общая сумма рассчитывается индивидуально.
Гипертермическая внутрибрюшинная химиотерапия сама по себе недешевая процедура, потому что она сложна, требует специального оборудования, соответствующей квалификации врача. За границей HIPEC будет стоить очень дорого, особенно в США, странах Европы, Израиле. Но в настоящее время этот вид лечения доступен и в России. Отечественные клиники используют современное оборудование от ведущих производителей, врачи проходят обучение у зарубежных экспертов и владеют методикой не хуже своих коллег из других стран. При этом в Москве можно пройти лечение по более низкой цене, чем за рубежом.
Например, в Москве гипертермическая внутрибрюшинная химиотерапия успешно проводится врачами в клинике MAMMA.
Дальнейшее развитие и другие разновидности методики
Подогретые растворы химиопрепаратов можно вводить не только в брюшную полость. Например, существует гипертермическая терапия под названием изолированная перфузия конечностей (isolated limb perfusion, ILP). Во время нее нагретый лекарственный раствор вводят в кровеносные сосуды руки или ноги. Это в ряде случаев помогает избежать ампутации конечности при саркомах мягких тканей, меланоме.
Более 20 лет известен метод гипертермической внутригрудной химиотерапии (hyperthermic intrathoracic chemotherapy, HITHOC). В данном случае препарат вводят в плевральную полость, окружающую легкие, для борьбы со злокачественным поражением плевры. Эта серозная оболочка похожа на брюшину, она выстилает стенки грудной полости и покрывает легкие.
Существует еще одна современная альтернатива HIPEC в лечении канцероматоза брюшины. Это внутрибрюшинная аэрозольная химиотерапия под давлением (pressurized intraperitoneal aerosol chemotherapy, PIPAC). Во время этой процедуры раствор химиопрепарата распыляют в виде спрея и впрыскивают под давлением в брюшную полость.
Продолжаются и научные исследования, посвященные HIPEC. Ученые оценивают ее эффективность в разных случаях, подбирают оптимальные препараты и протоколы, пытаются усовершенствовать методику и еще больше повысить ее эффективность, безопасность.
Проблемы методики HIPEC в России
В России HIPEC доступна, но лишь в очень немногих клиниках, и практически все они находятся в Москве. Широкому внедрению методики в онкологическую практику мешают три причины:
- Необходимость в квалифицированных врачах, умеющих проводить такое лечение и знающих все нюансы. Чтобы провести гипертермическую внутрибрюшинную химиотерапию, нужна целая бригада квалифицированного медперсонала.
- Очень дорогостоящее оборудование. Его может себе позволить не каждая клиника.
- Консервативность врачей. Доктора, особенно старшего поколения, неохотно принимают инновации. Некоторые считают, что эффективность и безопасность нового метода еще недостаточно изучены. Некоторые опасаются, что пары химиопрепаратов нанесут вред их собственному здоровью. Всё это мифы. Преимущества HIPEC давно доказаны многими научными работами.
Тем не менее гипертермическая внутрибрюшинная химиотерапия доступна в России, и жители нашей страны могут пройти этот вид лечения. Российские врачи применяют современное оборудование и после обучения и практики ни в чем не уступают своим западным и израильским коллегам. В клинике MAMMA есть все необходимое для проведения HIPEC и уже накоплен опыт ее успешного применения.

 Парковка для пациентов
Парковка для пациентов